我校基础医学院张春林教授团队的石海副教授主导完成的研究论文“DISCERN: Dual-Aptamer-Initiated Sensing Circuit via Engineered Nanozyme for Leukemia Stem Cells Phenotyping”,于2026年2月发表于国际期刊《ACS Sensors》(中科院一区TOP期刊,实时IF:10.4)。该研究开发了名为DISCERN的新型检测平台,通过双适配体启动的传感电路与工程化纳米酶组装,实现对白血病干细胞(LSCs)的高特异性、超灵敏表型分析,检测限低至8 cells/mL,为急性髓系白血病(AML)的复发预测和精准治疗提供了全新工具。

AML具有高度分子异质性,即使经过规范化治疗,仍有超过50%的患者发展为复发/难治性疾病。传统微小残留病(MRD)评估主要依赖多参数流式细胞术(MFC),但其灵敏度仅为0.1%~0.001%,且存在光谱重叠、设门主观等局限。值得注意的是,20%~70%的MFC-MRD阴性患者最终仍会复发。研究表明,化疗耐药性白血病干细胞(crLSCs)是驱动复发的核心因素,它们通过静止状态、代谢重编程等机制在化疗后潜伏下来。然而,现有方法难以对具有高度可塑性的LSCs进行可靠定量和表型分析。
为应对这一挑战,该团队开发了DISCERN(Dual-Aptamer-Initiated Sensing Circuit via Engineered Nanozyme)平台。这一名称蕴含巧妙的设计思路:让细胞自己“点亮”自己。DISCERN采用“与门”双适配体逻辑,同时靶向LSCs表面共表达的CD33和CD123。只有两个适配体结合到同一细胞时,通过邻近杂交形成纳米支架,触发滚环扩增(RCA)反应,在细胞表面扩增大量DNA长链;随后引导PCN-222(Fe)纳米酶定向组装,催化H₂O₂和TMB显色,产生从浅蓝到深普鲁士蓝的颜色变化。性能验证显示:检测限达8 cells/mL,线性范围为10~2000 cells/mL,检测时间约130分钟;对7种不同白血病细胞系的测试表明,仅CD33/CD123双阳性AML细胞产生明显信号,特异性较高。该平台还支持UV-vis光谱仪定量与智能手机RGB半定量双模式输出,并在药物诱导表型监测及小鼠异种移植模型血样检测中验证了其实用性。
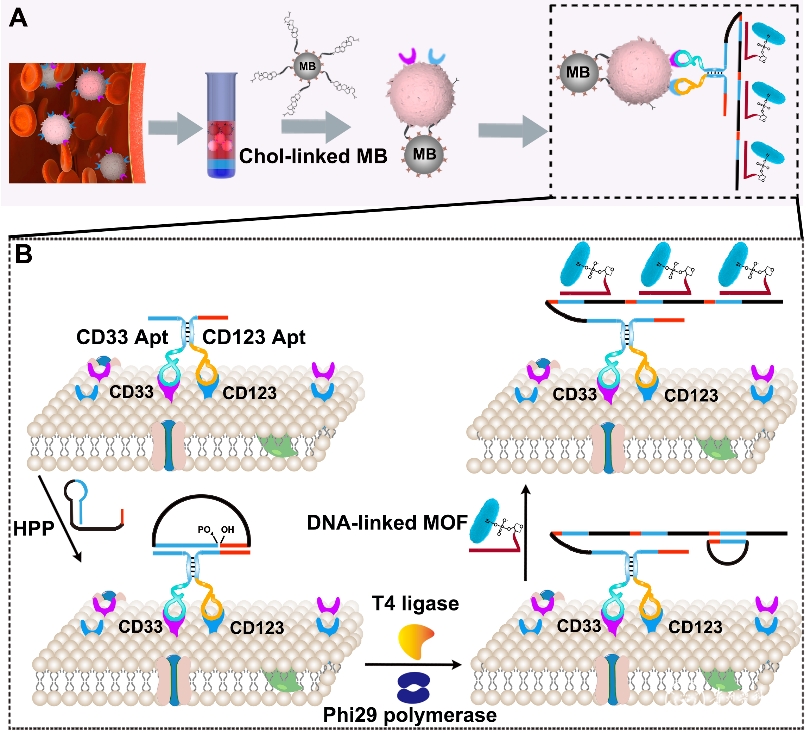
图示用于LSC比色表型鉴定的DISCERN平台示意图。(ACS Sens. 2026, 11, 1547−1556.)
基础医学院张春林教授与附属医院杨小燕教授为该论文的共同通讯作者,基础医学院石海副教授、硕士研究生刘璐为并列第一作者。基础医学院多名研究生及南京中医药大学博士研究生张斌参与该研究。我校分子医学工程研究中心和基础医学科学研究中心提供了仪器与技术支撑。该研究受国家自然科学基金(82202833、32360241)、贵州省科技厅项目(ZK[2024] general 139)、贵州省卫健委项目(2024GZYXKYJJXM0150)等资助。
原文链接:https://pubs.acs.org/doi/abs/10.1021/acssensors.5c03906
 公网安备 52010302000012号
公网安备 52010302000012号