近日,我校贵州省常见慢性疾病发病机制及药物研究重点实验室郭兵教授团队在Nature子刊《Nature Communications》(中科院1区Top期刊,IF:15.7)上发表研究论文“Adipocyte small extracellular vesicle-derived microRNA-30a-3p exacerbates hepatic steatosis in high fat diet-fed male mice”,揭示并阐明了脂肪组织通过细胞间信息传递调控肝脏脂质代谢的新机制,为代谢功能障碍相关脂肪变性肝病的防治提供了新的理论依据和潜在靶点。

代谢功能障碍相关脂肪变性肝病(MASLD)是当前全球最常见的慢性肝病之一,其核心特征是脂肪组织功能紊乱以及甘油三酯在肝脏中的异常积累。脂肪组织可分泌游离脂肪酸、脂肪因子及多种炎症因子,使肝脏更易受到脂毒性损伤并诱发代谢异常。然而,脂肪组织如何“远程”影响肝脏脂质代谢,其分子机制仍不清楚。因此,深入解析脂肪组织与肝脏之间的相互作用机制,对于探究MASLD的干预策略具有重要意义。
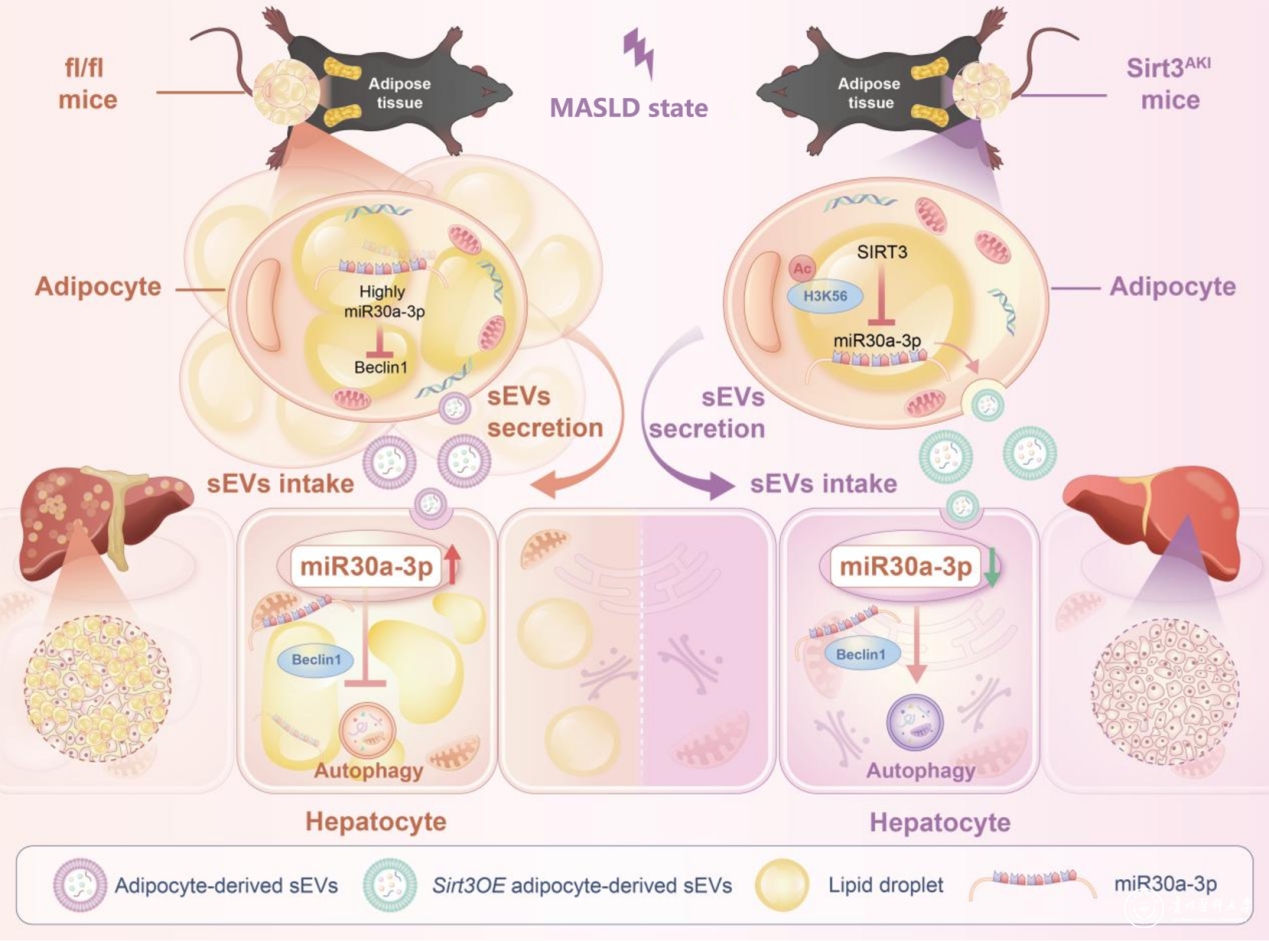
本研究发现,脂肪细胞可通过释放细胞外囊泡(small extracellular vesicles, sEVs),将关键调控分子miR-30a-3p传递至肝脏,通过抑制肝细胞自噬,加重肝脏脂质沉积和疾病进展。进一步研究表明,脂代谢紊乱时,脂肪组织中SIRT3表达降低,使其外泌体中miR-30a-3p增多,促进了MASLD发生发展。脂肪组织中的关键调控因子SIRT3通过调控表观修饰,抑制miR-30a-3p的产生,缓解肝细胞自噬受阻,从而减轻肝脏异位脂质沉积。此外,研究团队开发了一种靶向肝脏的工程化外泌体递送策略,通过将miR-30a-3p反义寡核苷酸(miR-30a-3p ASO)装载至sEVs中,高效地将miR-30a-3p ASO递送至肝脏,在动物模型中显著改善脂质代谢紊乱、胰岛素抵抗及肝功能损伤,实现了对致病miRNA的精准干预,并展现出良好的治疗潜力,为基于外泌体的精准治疗提供了重要实验依据。
该研究首次系统阐明了脂肪组织通过“sEVs-miRNA”途径与肝脏进行器官间通讯的分子机制,提出了“脂肪组织-肝脏轴”在MASLD发生发展中的重要作用。相关成果不仅加深了对脂肪肝发病机制的认识,也为开发靶向miR-30a-3p的新型治疗策略提供了重要理论基础。
本研究第一通讯单位为贵州医科大学中药功效成分发掘与利用全国重点实验室,由郭兵教授团队完成,并获得澳门大学林理根教授的大力支持。贵州医科大学基础医学院病理生理学教研室/贵州省常见慢性疾病发病机制及防治全省重点实验室张甜副教授为本论文的第一作者,病理生理学教研室硕士研究生胡龙堃、陈雕、博士研究生陈永鑫为本论文的共同第一作者。郭兵教授、澳门大学林理根教授、令狐克刚副教授为本论文共同通讯作者。该研究项目获国家自然科学基金等资助支持。
 公网安备 52010302000012号
公网安备 52010302000012号