近日,我校基础医学院分子医学团队在国际期刊《Advanced Composites and Hybrid Materials》(中科院1区Top期刊,IF:21.8)上发表研究论文“Dual-action selenium nanodrugs confer synergistic protection against Parkinson's Disease via mitochondrial-targeted antioxidant therapy and selenoproteinP-mediated selenium mobilization”,该研究开发并验证了一种基于谷胱甘肽修饰的硒纳米药物(G-Se NPs)的“双重作用”治疗策略:一方面,G-Se NPs通过血脑屏障,靶向神经元线粒体直接清除线粒体活性氧(mtROS);另一方面,通过调控肝脏合成硒蛋白P(SelP),经血脑屏障将硒(Se)输送至神经元,增强内源性抗氧化防御。这种“外源性清除+内源性动员”的协同机制,可为神经退行性疾病的治疗提供全新的潜在治疗策略。

帕金森病(PD)是常见的神经退行性疾病之一,罹患全球600多万人,目前尚无针对病因的有效治疗手段。线粒体功能障碍,特别是线粒体呼吸链缺陷所产生的过量mtROS,是导致多巴胺能神经元氧化应激的主要源头,被认为是驱动PD发病和进展的关键因素。然而,PD药物治疗面临的主要挑战是约98%的小分子药物和几乎所有大分子药物均无法有效穿过血脑屏障,严重制约了PD的药物治疗和候选药物来源。Se作为一种人体必需微量元素,已证实Se缺乏与多巴胺能神经元丢失密切相关,补充Se是治疗PD的有效策略,然而传统Se补充剂(如亚硒酸盐)存在剂量难以控制和严重的毒副作用等问题。因此,开发能够高效跨越血脑屏障的新型Se纳米药物,对于PD治疗具有重要意义。
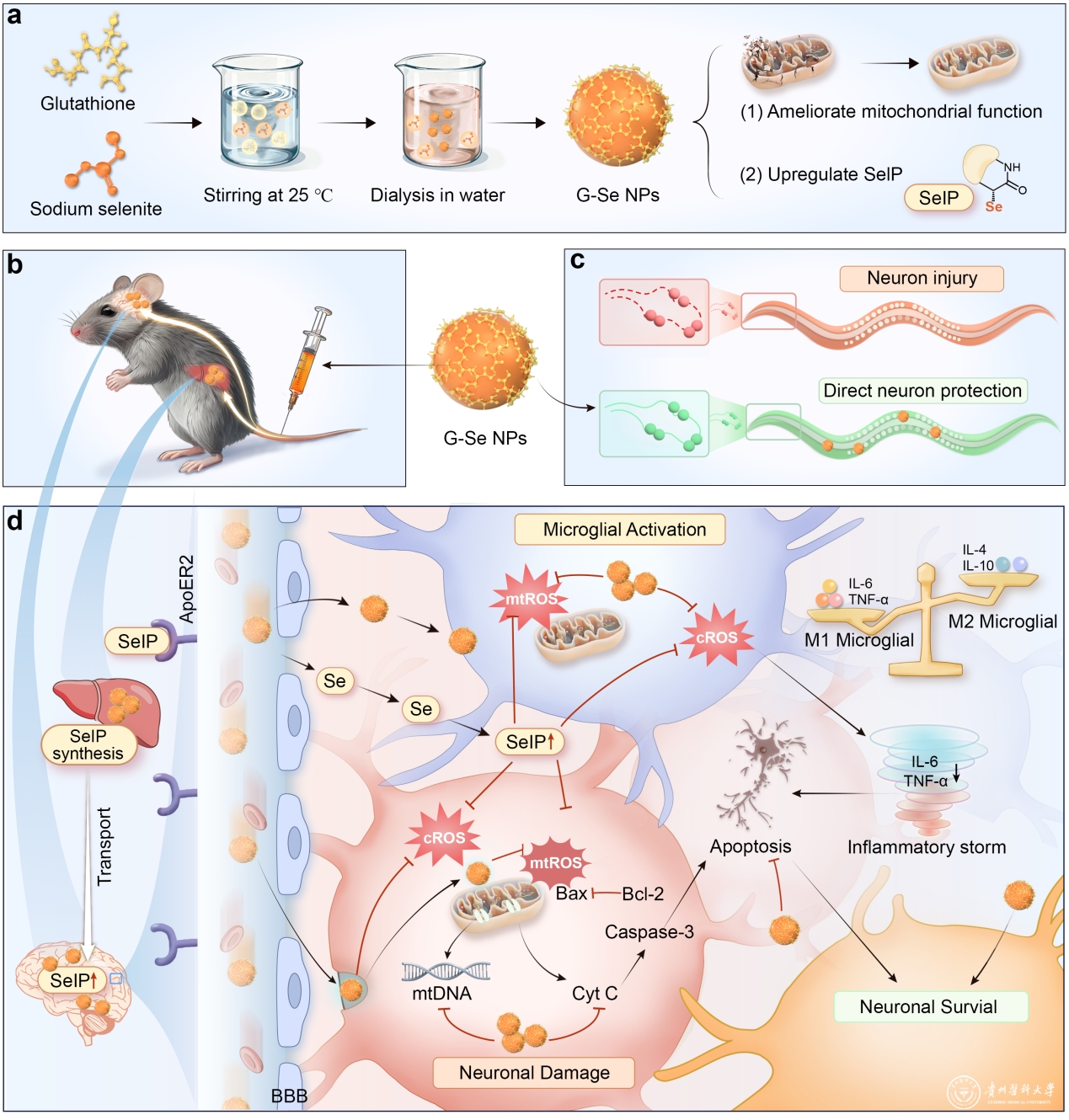
图示:纳米Se在PD的细胞、线虫和小鼠模型中的神经保护作用与机制示意图
本研究发现,硒纳米药物(G-Se NPs)可通过静脉注射,将活性硒(Se)递送至肝脏,通过上调肝脏中关键Se转运蛋白SelP的表达,SelP再经肝-脑轴输送至大脑,抑制神经元mtROS的产生并修复线粒体功能,从而减轻PD脑内氧化损伤及神经炎症。进一步研究表明,PD病理状态下,肝脏中SelP的合成与分泌受到抑制,导致脑内Se供应不足及相关硒蛋白合成减少。为此,G-Se NPs还能够直接通过血脑屏障,高效地将Se递送至多巴胺能神经元,并上调内源性相关硒蛋白表达。G-Se NPs实现了对PD多巴胺能神经元直接的mtROS清除和间接的内源性抗氧化系统修复。
本研究的主要通讯单位是贵州医科大学基础医学院/贵州省医学分子生物学重点实验室、贵州医科大学中药功效成分发掘与利用全国重点实验室。该研究获得中国科学院上海药物研究所于海军研究员的大力支持,以及国家自然科学基金的资助。
雷莉副教授(贵州医科大学基础医学院)、宋凌励(细胞生物学专业硕士研究生)、敖启航(2023级协和班本科生)为本论文的共同第一作者。张春林教授、汤磊教授、于海军研究员为本论文的共同通讯作者。
 公网安备 52010302000012号
公网安备 52010302000012号