近日,贵州医科大学中药功效成分发掘与利用全国重点实验室罗成团队与上海药物所周虎团队、福建师范大学林华团队合作,创造性开发出一种名为光诱导的天冬氨酸到丙氨酸蛋白编辑剂(light-induced Asp(D)-to-Ala(A) protein editors, LIDAPEs)的全新技术,筛选并发现可用于蛋白质精准编辑的公共化学骨架,通过将化学编辑片段(光催化弹头,warhead)与靶向识别单元(binder)整合为双功能小分子,首次在活细胞中实现了对目标蛋白特定氨基酸位点的精准定点编辑。该研究将非共价的小分子化合物从传统的“物理占据”升级为“化学改性”,为未来开发出新形态药物-基于蛋白编辑的化学药物提供了全新的理论依据和可行的技术路径。
2026年4月1日,该工作以“Small-Molecule–Mediated Precision Protein Editing in Living Cells”为题,发表在Vita上。

如何在不改变基因序列的前提下,直接对内源性天然蛋白进行位点特异性的单氨基酸编辑,一直是化学生物学领域的关键技术瓶颈。尽管基因组编辑技术的发展已深刻变革生物学研究范式,但目前仍缺乏能够直接在天然蛋白质层面进行定点编辑的工具。已有基于内含肽的蛋白编辑策略仍需借助基因改造实现蛋白修饰,无法实现对内源蛋白的直接编辑,也难以精准靶向特定氨基酸残基。因此,长期以来领域认为利用小分子实现对蛋白质的精准编辑,虽然意义重大,但难度极大,几乎不可实现。
针对天然蛋白质难以直接编辑的挑战,该研究从化学反应原理出发,尝试解决生物学难题。研究团队受天然酶在光照条件下催化脂肪酸脱羧氢化反应的启发,设计了一类可定点编辑酸性氨基酸残基的小分子化合物,最终开发出名为光诱导的天冬氨酸到丙氨酸蛋白编辑剂(LIDAPEs)的技术。团队以CDK2为靶标蛋白质模型进行了结构导向的理性设计,将靶向识别单元(binder)与筛选并理性设计的全新光催化弹头(warhead)巧妙融合,获得了高效编辑分子LL-DA-3,光照条件下能以高达86.7%的编辑效率,精准地将CDK2的DFG基序中D145位点转化为丙氨酸(D145A)。更为难得的是,该反应对蛋白中其他酸性残基及氧化还原电位更低的C末端羧基几乎无脱靶效应,展现出优异的编辑选择性。此外,该分子同样可在CDK12和FGFR2等不同激酶中实现对DFG基序中天冬氨酸的定点编辑,初步揭示了该技术的普适性。
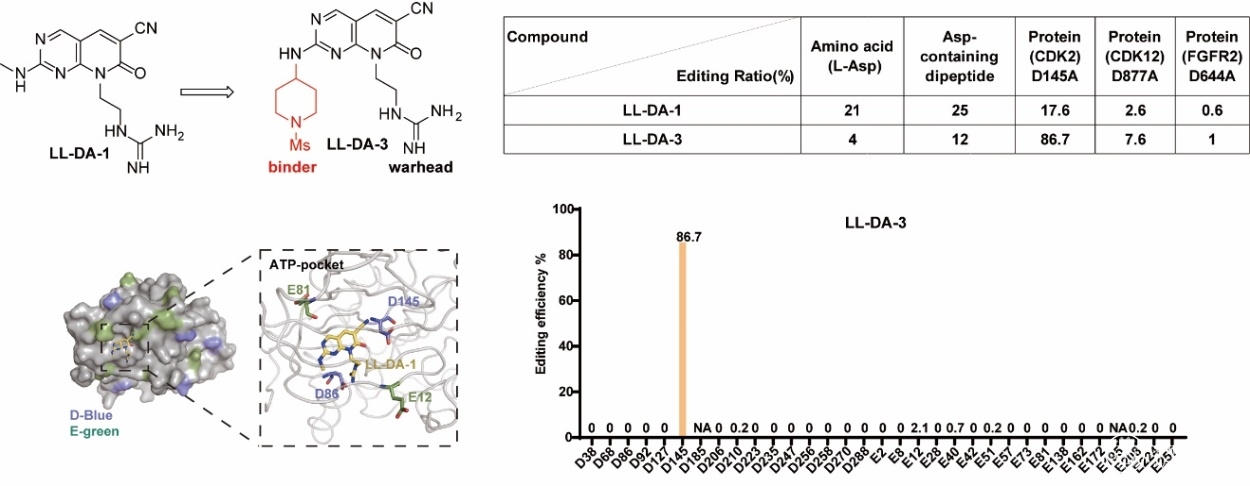
高编辑效率与编辑选择性小分子LL-DA-3的设计与确证
为揭示其高效、高特异性编辑的底层逻辑,研究团队解析了LL-DA-3与CDK2的复合物晶体结构,并结合量子化学计算进行了深入探究。研究揭示了其分子机制:LL-DA-3通过占据CDK2的ATP结合口袋,在光照条件下触发自由基脱羧氢化反应。该过程通过水分子介导的氢键网络实现电子与氢质子的精准传递,使D145的侧链羧基发生脱羧氢化反应,最终转化为甲基,实现D145A的特异性转化。值得注意的是,在HEK-293T活细胞体系中,LL-DA-3同样能实现对CDK2蛋白D145位点的原位编辑,证明该技术在复杂生物环境中的适用性。
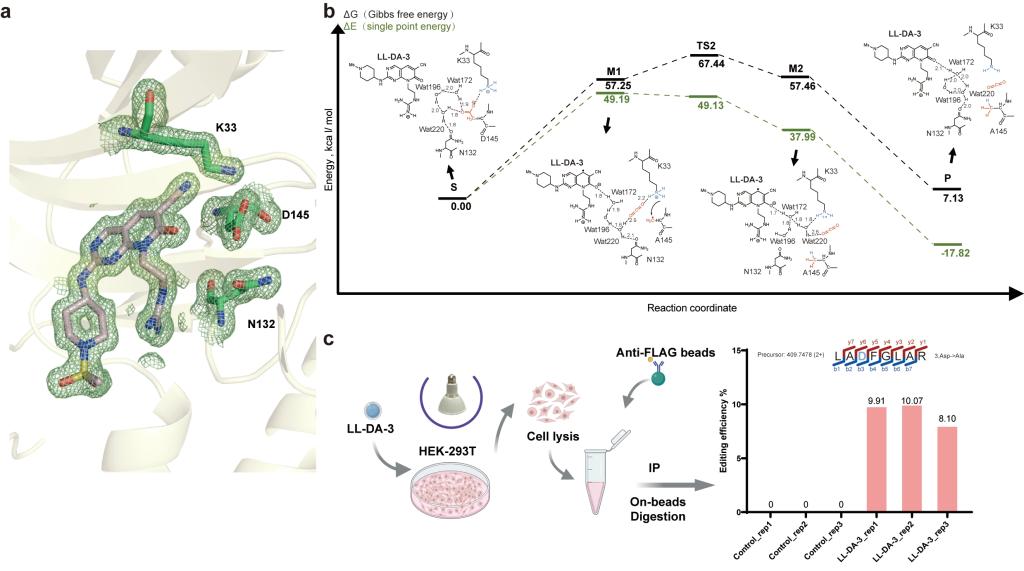
LL-DA-3的作用机制与活细胞中编辑效率探索
贵州医科大学、中药功效成分发掘与利用全国重点实验室/上海药物研究所罗成团队长期致力于化学生物学新技术、新方法的开发,靶向生物大分子动态修饰的开发,在创新药物早期发现取得系列研究进展(Nature 2021; Cancer Cell 2023; Mol Cell 2023; Nat Methods 2025; Nature Commun 2022/2023/2024a/2024b/2025;JACS 2025/2026;Angew Chem Int Ed Engl 2021/2025)等。近年来,团队研究已经逐步从靶向蛋白质修饰、利用化学修饰实现对蛋白质干预,聚焦到实现靶向特定蛋白质的精准化学编辑技术开发和应用。该工作的第一通讯单位为贵州医科大学,通讯作者为罗成研究员、林华研究员与周虎研究员,本研究得到了国家蛋白质中心(上海)、上海同步辐射光源的支持,获得了国家重点研发计划、国家科技重大专项、国家自然科学基金、中药功效成分发掘与利用全国重点实验室等项目的资助。
 公网安备 52010302000012号
公网安备 52010302000012号